Gubelin Harcha W. et al. — Journal of the American Academy of Dermatology, 2014
Voir l'étudeLa dihydrotestostérone (DHT) est le principal androgène responsable de l'alopécie androgénétique, une pathologie ayant des répercussions psychologiques et physiques qui justifie une prise en charge médicale.
Comparer l'efficacité et la sécurité du dutastéride (inhibiteur des 5-alpha réductases de types 1 et 2) à celles du finastéride (inhibiteur de la 5-alpha réductase de type 2) et d'un placebo chez des hommes atteints d'alopécie androgénétique.
Étude sur 24 semaines : Comparaison du dutastéride (0,02 à 0,5 mg), du finastéride (1 mg) et d'un placebo chez des hommes de 20 à 50 ans. Critères d'évaluation : densité capillaire (critère principal), diamètre des cheveux, analyses photographiques et impact sur la qualité de vie.
Sur 917 participants, le dutastéride a montré une efficacité dose-dépendante. À 0,5 mg, il a surpassé de manière significative le finastéride et le placebo en termes de densité, de diamètre et de repousse capillaire à 24 semaines. La tolérance est restée comparable entre tous les groupes.
L'étude était limitée à 24 semaines.
Le dutastéride a augmenté la croissance et la restauration capillaires chez les hommes atteints d'alopécie androgénétique et a été relativement bien toléré. (J Am Acad Dermatol 10.1016/j.jaad.2013.10.049.)
La calvitie masculine — appelée alopécie androgénétique — est l’une des formes de chute de cheveux les plus répandues. Elle est provoquée par une hormone, la dihydrotestostérone (DHT), qui attaque progressivement les follicules pileux chez les hommes génétiquement prédisposés. Au-delà de l’aspect esthétique, cette condition peut avoir un impact réel sur la confiance en soi et la qualité de vie.
Deux médicaments permettent de freiner ce processus en bloquant la production de DHT :
• La finastéride (1 mg/j), utilisée depuis de nombreuses années, bloque un seul type de l’enzyme responsable de la DHT (le type 2).
• Le dutastéride, plus récent, est potentiellement plus puissant car il bloque deux types de cette enzyme à la fois (types 1 et 2), réduisant ainsi davantage la DHT dans l’organisme.
Pourtant, aucune grande étude n’avait encore comparé directement ces deux traitements. C’est précisément l’objectif de cet essai clinique.
Cette étude a recruté 917 hommes entre 20 et 50 ans, tous atteints de calvitie, dans 39 centres médicaux répartis dans 9 pays (dont le Japon, le Chili, Taïwan et la Russie). Elle a été conçue de manière très stricte : ni les patients ni les médecins ne savaient quel traitement chacun recevait (étude dite « en double aveugle »), ce qui garantit des résultats fiables et non influencés.
Les 917 participants ont été répartis aléatoirement en 5 groupes pendant 24 semaines (6 mois) :
Au début de l’étude, les 5 groupes étaient parfaitement comparables : même âge moyen (environ 38 ans), même degré de calvitie, et même nombre de cheveux de départ (environ 760 cheveux dans la zone analysée). La grande majorité des participants (55 %) étaient d’origine asiatique, 40 % hispanique et 5 % caucasienne.


Pour évaluer l’efficacité des traitements, les chercheurs ont utilisé plusieurs outils complémentaires :
Après 24 semaines, voici combien de cheveux supplémentaires ont été gagnés en moyenne dans la zone analysée (cercle de 2,54 cm au vertex), par rapport au début de l’étude :
Le dutastéride 0,5 mg a donc permis de gagner 33 cheveux de plus que la finastéride dans cette zone, soit une efficacité supérieure de 58 % par rapport au traitement de référence. Ces résultats étaient statistiquement significatifs (P = 0,003), ce qui signifie que la différence n’est pas due au hasard.
Sur une zone plus petite (cercle de 1,13 cm, qui représente le cœur de la zone touchée), les résultats étaient similaires : le dutastéride 0,5 mg donnait +18,1 cheveux, contre +12,1 pour la finastéride et −0,3 pour le placebo.

Au-delà du nombre, les chercheurs ont mesuré l’épaisseur des cheveux (en micromètres, μm). Voici les variations observées à 24 semaines :
Cette mesure est importante : des cheveux plus épais donnent visuellement davantage de volume et de densité. Le dutastéride 0,5 mg améliorait ainsi l’épaisseur des cheveux de façon significativement supérieure à la finastéride (P = 0,004).

Un jury de 3 dermatologues indépendants a évalué les photos « avant/après » de chaque patient sur une échelle allant de −3 (très aggravé) à +3 (très amélioré). Les scores moyens obtenus à 24 semaines étaient :
Concrètement, en regardant le détail des évaluations (Tableau II), voici la proportion de patients dont la calvitie s’est améliorée au vertex à 24 semaines :
Ces résultats confirment que l’amélioration mesurée en laboratoire se traduit bien par une différence visible à l’oeil nu, particulièrement pour la région frontale où le dutastéride 0,5 mg était supérieur à la finastéride (P = 0,002).



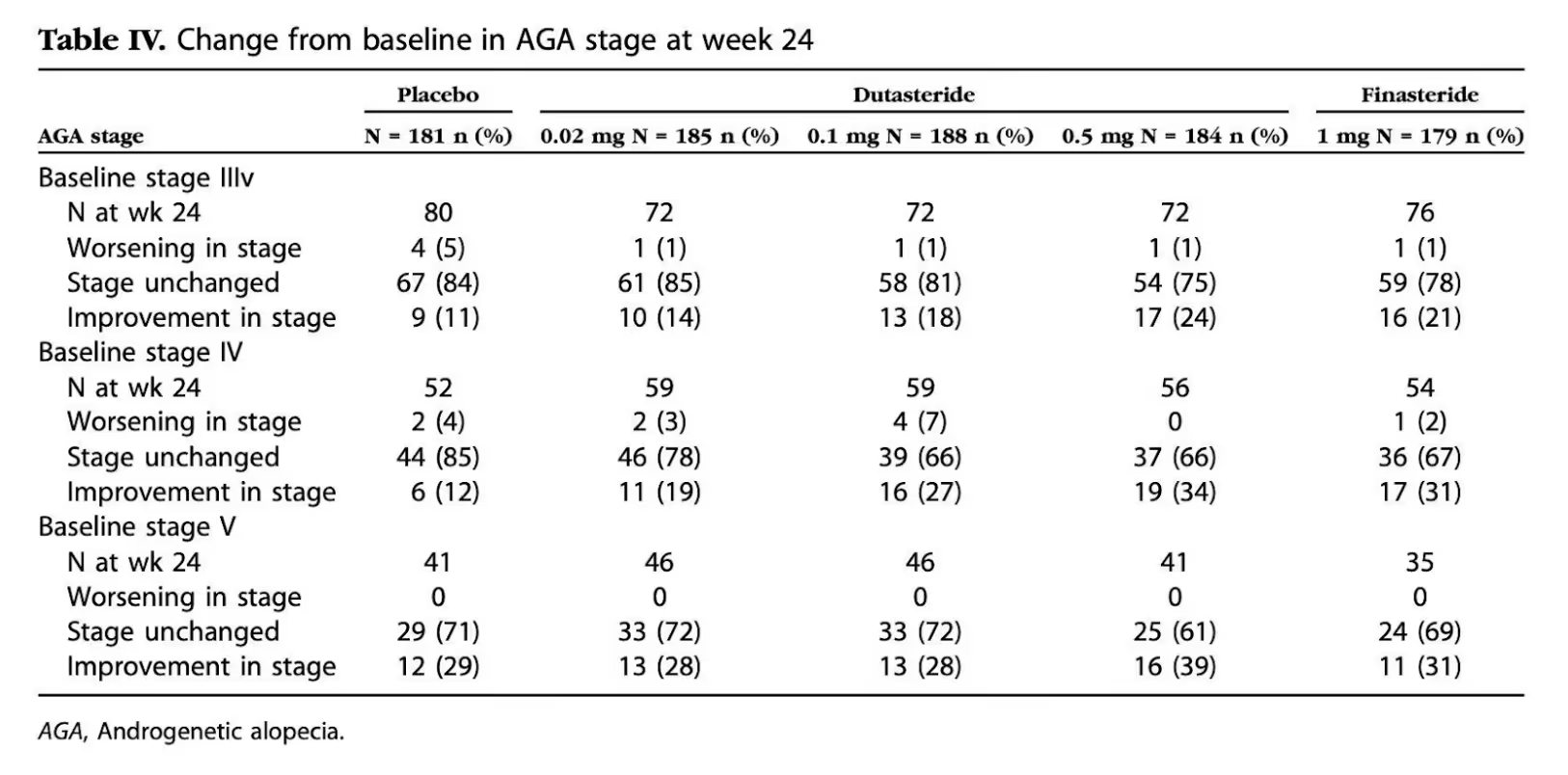
Les médecins ont également suivi l’évolution du stade de calvitie de chaque patient. Le tableau ci-dessous décrit les résultats selon le stade de départ.
Patients démarrant au stade III vertex (calvitie débutante au sommet) :
Patients démarrant au stade IV (calvitie avancée) :
Patients démarrant au stade V (calvitie sévère) :
Ce qui est remarquable ici, c’est qu’aucun patient sous dutastéride 0,5 mg n’a connu d’aggravation de stade, quel que soit le stade de départ.
Au-delà des mesures objectives, les patients ont été interrogés sur leur ressenti via deux questionnaires validés scientifiquement. Les résultats étaient clairs :
Autrement dit, les patients qui prenaient du dutastéride étaient non seulement objectivement plus chevelus, mais ils le ressentaient aussi et en étaient plus satisfaits au quotidien.
C’est la question essentielle quand on compare deux médicaments. Voici ce que l’étude a observé :
Effets secondaires globaux (Tableau V) :
L’incidence globale des effets indésirables était similaire dans tous les groupes : environ 49 à 54 % des participants ont signalé au moins un effet indésirable, ce qui peut paraître élevé mais inclu des incidents banalissimes comme un rhume ou un mal de tête. Le taux était comparable au placebo (52 %), ce qui confirme que la plupart de ces événements n’étaient pas liés au médicament.

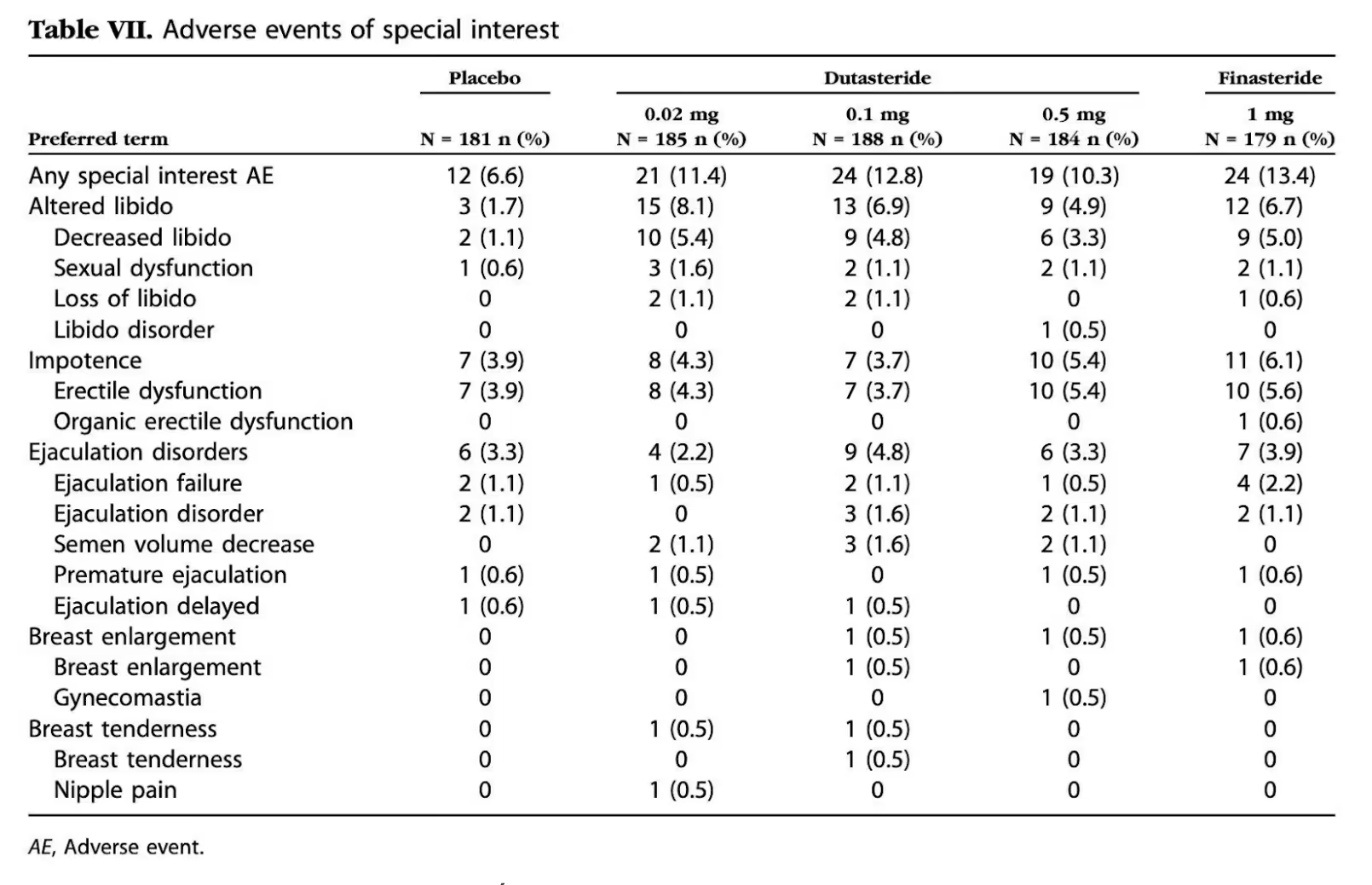
Effets sexuels (Tableau VII) :
C’est le point de vigilance le plus important pour ces traitements. Les problèmes de libido concernés :
Pour les troubles de l’érection : environ 3,7 à 5,6 % des patients selon le groupe, contre 3,9 % sous placebo — des chiffres comparables. Aucune relation dose-réponse n’a été observée avec le dutastéride, ce qui signifie que prendre une dose plus élevée n’augmentait pas le risque d’effets sexuels.
Arrêts de traitement (Tableau VI) :
Très peu de patients ont dû arrêter le traitement en raison d’effets indésirables : 3 % sous placebo, 4 % sous dutastéride 0,1 mg, 3 % sous dutastéride 0,5 mg, et 2 % sous finastéride. Les principales causes d’arrêt étaient les troubles érectiles et la baisse de libido, mais toujours dans de très faibles proportions (1 à 2 % des patients).
Fait rassurant : aucun cas de cancer de la prostate, de cancer du sein ni d’événement cardiovasculaire attribué aux traitements n’a été rapporté

Au-delà des mesures objectives, les patients ont été interrogés sur leur ressenti via deux questionnaires validés scientifiquement. Les résultats étaient clairs :
Autrement dit, les patients qui prenaient du dutastéride étaient non seulement objectivement plus chevelus, mais ils le ressentaient aussi et en étaient plus satisfaits au quotidien.
Cette étude est la première à comparer directement le dutastéride et la finastéride dans le traitement de la calvitie masculine sur un aussi grand nombre de patients.
Ses conclusions sont nettes :
En pratique, le dutastéride représente une option thérapeutique sérieuse et plus efficace que le finastéride pour les hommes souffrant de calvitie. Comme pour tout médicament, son utilisation doit être discutée avec un médecin.
Extrait de Télématin, France 2 — diffusé le 6 mai 2026